定制您的临床研究方案
联系定制

放射性药物(以下简称“核药”)是一种利用放射性同位素标记的药物,通过放射性核素的辐射来实现医学诊断和治疗的用途。核药并不是一个全新的概念,早在20世纪初批准的131I和18F-FDG,依然是核医学科用于甲状腺疾病诊疗和PET-CT肿瘤诊断的重要药物。2013 年,随着拜耳的Xofigo®(233Ra)获批上市,诺华收购AAA公司的68Ga(NetSpot®)和177Lu(Lutathera®)标记的靶向放射性诊疗一体化药物,使靶向核药正式走进创新药领域,发展为“黄金”赛道。在谈核药申报之前,我们先来了解下核药及其特点。
核药一般由放射性同位素搭配专门定位特定器官及组织的分子试剂组成,放射性核素发生核衰变时释放α、β和γ粒子,产生电离辐射,从而实现显像或者治疗的目的。根据用途,核药可分为诊断用核药、治疗用核药和诊疗一体化核药,释放α粒子、β粒子的核素通常用于治疗,释放γ粒子的核素通常用于诊断。
结合SPECT或PET采用示踪技术,在分子水平上研究药物在活体内的功能和代谢过程,实现生理和病理过程的快速、无损和实时成像,为真正意义上的早期诊断、及时治疗提供了手段。常见的诊断用核素包括99mTc、123I和131I等。
可高选择性浓集在病变组织,利用放射性同位素在衰变过程中释放的各种射线产生局部电离辐射生物效应,从而抑制或破坏病变组织发挥治疗作用。常见的治疗用核素包括137Cs、192Ir和90Y等。
基于不同核素半衰期及发射射线的特点,用不同核素探针将显像诊断与辐射治疗相结合,达到可视化诊断与精准治疗的目的。诊断性核药通过分子影像显示病灶,治疗性核药通过分子标记等手段被病灶靶向摄取,通过辐射治疗成像病灶,真正实现个体化的诊断与治疗。RDC是临床实操中能够实现诊疗一体化的药物,相同靶向配体和连接子的RDC分子既可以与释放γ射线的诊断核素结合,也可以与释放α和β射线的治疗核素相结合。
核药具有“核”与“药”双重属性,其特点主要体现在:
具有放射性;
特定的半衰期;
极微的化学剂量;
通常定制生产或即时标记;
按放射性活度给药;
特殊的质量控制方法等。
这些特点决定了核药在研发、生产、放行、运输和使用等管理程序上都存在较高的技术壁垒,对创新药研发带来了更多的挑战。
与普药(非放射性药物)相比,核药在临床上存在多重优势,主要体现在:
诊断类核药,可实现诊断可视化且敏感度高,如通过PET-CT可直观显示AD患者中是否有斑块及斑块位置和密度;
核药依靠核素衰变产生的辐射实现治疗的目的,可降低病灶的放射抵抗的耐药机会,具有精准治疗、不易耐药的优势;
可个体定量化,如医生可根据患者肿瘤病灶大小调整给药剂量,保证疗效的同时降低不良反应比;
适用范围广,根据不同核素特点可用于肿瘤、心血管和自身免疫性等疾病的诊疗。
基于核药在精准治疗和诊疗一体化方面的这些无可比拟的优势,核药在临床应用方面的需求量正在逐年上升,这为核药特别是靶向性核药的快速发展奠定了基础。
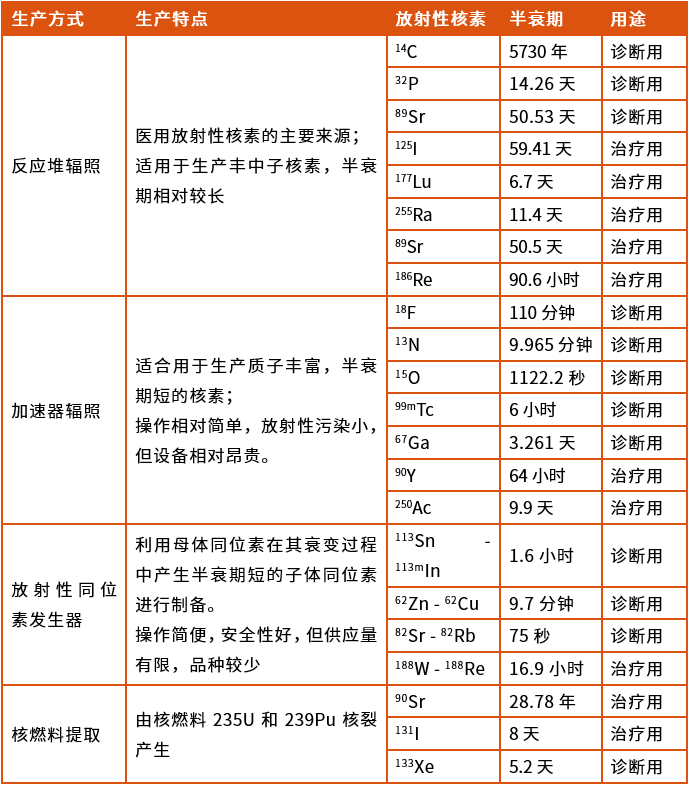
核素生产是核药行业的基础,其质量和产量直接影响到下游产品的质量和应用。目前放射性核素的主要生产方式有反应堆辐照、加速器辐照、放射性同位素发生器、核燃料提取四种方式。但我国医用放射性核素短缺,研制仍在很大程度上依赖进口。
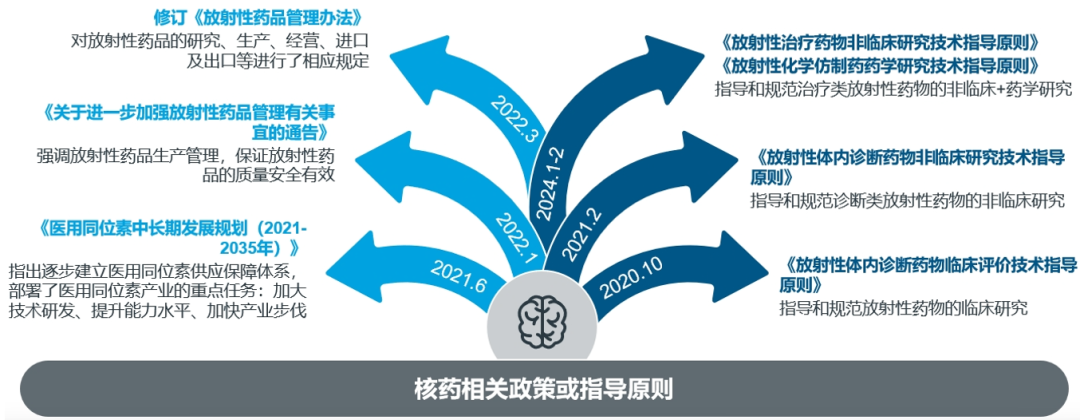
2021年,国家原子能机构联合多个部门正式发布了《医用同位素中长期发展规划(2021—2035年)》,这是我国首个针对核技术在医疗卫生应用领域发布的纲领性文件,鼓励医用同位素制备技术研究、放射性新药研发等多项研究创新发展。自此,我国核素自主化研制进入了良性发展阶段,131I、177Lu、89Sr等多种核素已实现自主供给。此外,药品监管机构也发布了一系列鼓励核药发展的相关政策和指导原则,推动创新核药研发进入到快速上升期。
从核药注册申报的角度,2023年4月25日国家药监局发布《关于改革完善放射性药品审评审批管理体系的意见》,明确提出鼓励核药研发注册、优先审评机制、完善技术评价体系,此意见更是为核药申报提供了更为明晰的支持路径。但是由于核药的特殊性,使其不仅在研发生产方面存在较高的技术壁垒,在注册申报方面也存在很多特殊性。核药申报系列下文将基于昆拓注册事务部的申报经验,从注册角度剖析核药研发和申报的注意事项。
作者:LL Yang
昆拓信诚医药研发(北京)有限公司,成立于2011 年,在北京、上海、广州、成都、杭州、合肥设有办公室,拥有全国近1000名员工。昆拓是 IQVIA(艾昆纬)专为中国本土设立的临床研究服务机构,致力于为制药企业和医疗器械及体外诊断试剂公司提供优质可靠的临床研究服务。临床研究服务包括:研究中心管理CRC服务、临床委派FSP、临床监查、项目管理、医学事务、生物统计、数据管理、注册事务、药物警戒、医学翻译、质量管理和质量保证等。从成立至今,昆拓已经为多家国内外知名药械公司提供了各项临床研究服务超过1300项,为客户开发定制解决方案,帮助中国本土和全球生物制药及器械公司在中国成功注册新产品。